日前,未知君与华西医院在慢性免疫疾病领域的重要科研合作成果——《Eubacterium rectale is a potential marker of altered gut microbiota in psoriasis and psoriatic arthritis(编者译:Eubacterium rectale是银屑病和银屑病关节炎患者肠道微生物群改变的潜在生物标志物)》,在Microbiology Spectrum正式发表,揭示了E. rectale有望成为银屑病诊断标志物和治疗干预的靶点。
近年研究发现,肠道菌群-免疫-皮肤轴三者的相互关系,对于维持宿主免疫平衡和健康至关重要,在皮肤疾病的发生和发展中起到重要作用。前期关于银屑病的肠道菌群研究,缺乏大规模的人群调查以及高分辨率的菌群检测方法。本研究招募了44例斑块状银屑病(PsO)患者和26例银屑病关节炎(PsA)患者,以及年龄、性别匹配的26名健康对照(HC)进行横断面研究,利用高深度的宏基因组测序技术,刻画了PsO和PsA患者的肠道微生态特征。
PsO是一种常见的慢性免疫相关皮肤病,有许多合并症,而PsA就是其中之一,约有30%的PsO患者会逐渐发展为PsA。目前,PsO的发病机制复杂且尚未明确,其中辅助T细胞(Th)-17/白细胞介素(IL)-23轴被确定为其关键的免疫机制。同时,已有多条证据表明,肠道菌群在维持宿主免疫稳态方面至关重要,尤其是影响调节性T细胞和效应性T细胞的平衡。
通过分析PsO和PsA患者中肠道菌群的组成和功能特征,未知君与华西医院的研究者发现,与健康人相比,PsO和PsA患者的肠道菌群多样性降低。此外,通过对年龄、性别、BMI指数等协变量进行矫正,及利用PERMANOVA检验的结果也显示,与健康人相比,银屑病患者的肠道微生物组成发生了显著变化。但在PsO和PsA患者之间没有观察到这种差异。在不同的组别的功能通路注释分析中,也印证了上述的结论。
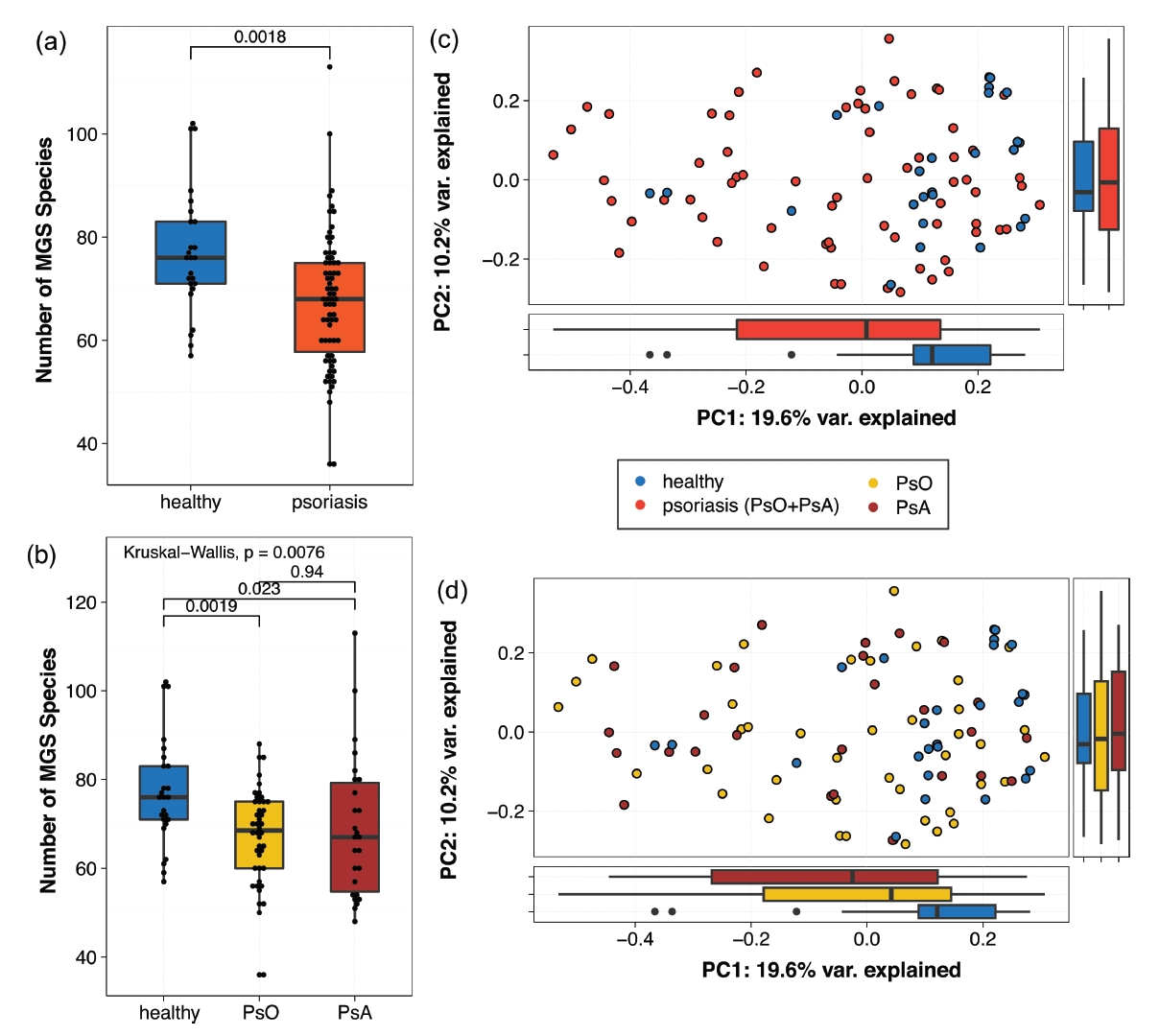
与年龄匹配的健康对照组相比,患者肠道微生物组成发生变化
接着,研究者利用多种生物信息分析方法找到了多个在银屑病患者肠道中明显缺失的微生物,包括E. rectale、Alistipes和Bacteroides菌属中的多个物种。其中,E. rectale缺失情况最为严重:银屑病患者的肠道内存在E. rectale定植的概率不足健康人肠道内该物种定植的1/50。此外,在基于Kegg数据库注释进行的功能通路差异分析中,E. rectale主要贡献的淀粉和蔗糖代谢、细菌趋化性、丁酸代谢三个功能途径,在银屑病患者中也显著降低。这些基因功能的差异在进一步对物种基因和直系同源基因的分析中得到了反复印证。物种、基因、功能的多方印证可能表明在肠道中存在着以E. rectale为核心的生态功能单元,这一生态功能单元的缺失可能是银屑病发病的潜在原因。
更进一步,研究者推测E. rectale可以作为有效区分银屑病患者和健康者的生物标记物,这一猜测也在后续的ROC模型曲线中得到了验证。为了得到更切实的证据,研究者还通过对宏基因组数据进行基因组组装分箱和巢式PCR实验验证的方式,确定了E. rectale在患者肠道中的缺失,以及在健康者肠道中的富集。
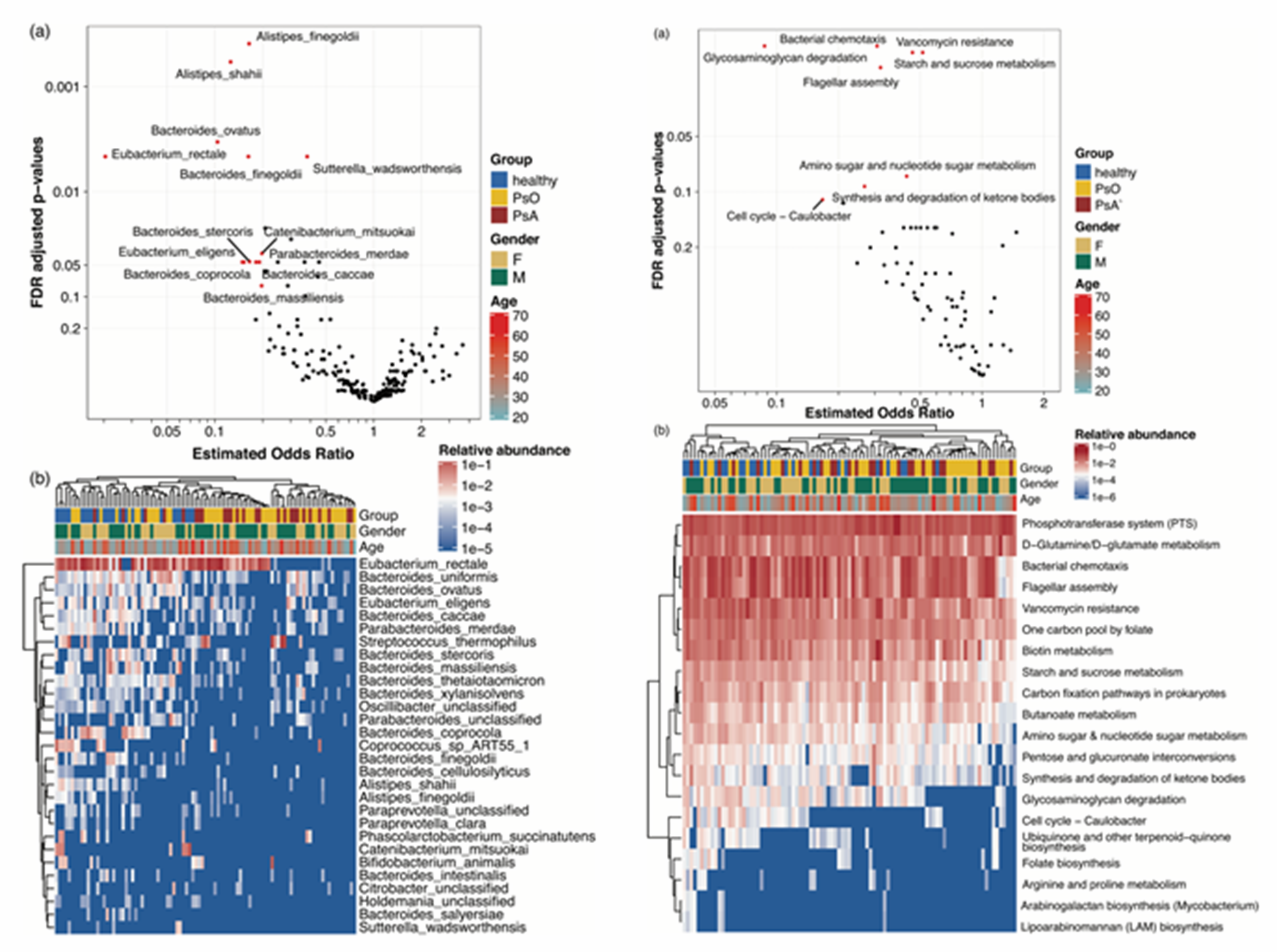
此前报道的各项研究中,免疫相关的生物制剂治疗对肠道微生物的影响存在不一致的结论。为此,研究者对接受Secukinumab/Adalimumab治疗的22名银屑病患者进行了持续随访,并探讨了疗前肠道菌群与治疗效果之间的关系。结果显示,患者治疗前的肠道菌群似乎没有影响Secukinumab/Adalimumab治疗的疗效。
综上所述,此项研究发现了E. rectale作为肠道微生物群中重要的生态功能单元,为开发新的疾病预防和治疗策略提供重要的理论依据。该研究发现将极大助力未知君基于微生态的创新药物研发、FMT精准供体选择和益生菌产品开发。通过调节肠道菌群健康、维持免疫平衡,从而促进皮肤健康,将成为预防和治疗皮肤疾病的新策略。
原文链接: https://journals.asm.org/doi/10.1128/spectrum.01154-23
-End-